作者简介: 杨辉(1963-),男,广西桂林人,副主任药师,主要研究方向:药品检验、质量标准研究。电话:0771-3100835,E-mail:yh07719001@21cn.com。
目的 建立超高效液相色谱(UPLC)法同时测定复方黄根颗粒中齐墩果酸和没食子酸的含量。方法 采用Agilent Eclipse Plus C18色谱柱,以甲醇-0.1%磷酸溶液为流动相,梯度洗脱,流速:0.2 mL·min-1,波长切换,0~7 min波长270 nm测定没食子酸,7~14 min波长 215 nm测定齐墩果酸。结果 没食子酸和齐墩果酸溶液分别在0.022 06~0.198 54 mg·mL-1( r=0.999 6, n=5),0.031 04~0.279 36 mg·mL-1( r=0.999 8, n= 5)范围内与峰面积积分值呈良好线性关系,平均回收率分别为100.20%和99.96%;RSD分别为0.45%和0.64%。结论 该方法操作简便、重复性好,可以更有效地控制制剂的质量。
Objective To establish an UPLC method for content determination of gallic acid and oleandic acid in compound Huanggen granules.Methods Agilent Eclipse Plus C18 column was used with the mobile phase of methanol-0.1% phosphoric acid by gradient elution.Flow rate was 0.2 mL·min-1.Detection wavelength was set at 270 nm in the first 7 min for gallic acid and then changed to 215 nm for oleandic acid between 7 and 14 min.Results The linear concentration ranges of gallic acid and oleandic acid were 0.022 06-0.198 54 mg·mL-1( r=0.999 6, n=5) and 0.031 04-0.279 36 mg·mL-1( r=0.999 8, n=5).Their average recovery was 100.20% (RSD=0.45%)and 99.96%(RSD=0.64%),respectively.Conclusion The extablished method is simple,reproducible and specific, and can be use to the quality control of compound Huanggen granules.
复方黄根颗粒是由广西平乐县中医医院根据传统壮族医药新研制开发生产的院内制剂,由黄根、叶下珠、三叶香茶菜、三七、黄芪、白术、绞股蓝等7味药组成[1,2,3,4]。本制剂具有祛瘀生新、利湿退黄、平肝清热、保肝降酶、利水解毒和抗肝纤维化的作用,临床用于治疗不同证型的慢性乙型肝炎、脂肪肝、酒精性肝病等肝病具有较好的功效[5,6,7]。原质量标准仅对制剂的性状、颗粒剂项下有关各项规定进行检验,没有对制剂中有效成分进行含量测定[2]。为更好地控制药品质量,笔者参考相关文献报道[8,9,10,11],建立超高效液相色谱(ultra performance liquid chromatography,UPLC)双波长切换同时测定制剂中没食子酸和齐墩果酸含量的方法,报道如下。
美国Agilent 1290高效液相色谱仪(二极管阵列检测器);AE240电子天平(梅特勒-托利多仪器公司,感量:0.01 mg);KQ-300型超声波清洗器(江苏昆山市超声仪器有限公司)。
没食子酸(批号:110831-200803,含量:90.1%),齐墩果酸(批号:110709-200304),均购自中国食品药品检定研究院;甲醇为色谱纯,水为高纯水,其他试剂均为分析纯。 实验用药材由广西平乐县中医医院提供,并经本所中药室鉴定为现行药品标准收载品种;复方黄根颗粒(广西平乐县中医医院制备,规格:每袋3 g,批号:20130311,20130326,20130403,20130512,20130521,20130610)。
色谱柱:Agilent Eclipse Plus C18柱(100 mm×2.1 mm,1.8 μm );流动相:甲醇(A)-0.1% 磷酸溶液(B),梯度洗脱;0~7 min,20% A,~14 min,20% A→80%A;流速:0.2 mL·min-1;柱温:30 ℃;进样量:2 μL;检测波长:波长切换,0~7 min在270 nm波长测定没食子酸含量,7~14 min在215 nm波长测定齐墩果酸含量。
2.2.1 对照品溶液 分别精密称取干燥至恒重的没食子酸、齐墩果酸对照品12.24,15.52 mg,分别置50 mL棕色量瓶中,加50%甲醇溶解并稀释至刻度,摇匀,即得浓度分别为0.220 6 mg·mL-1和0.310 4 mg·mL-1对照品储备液。
对照品混合溶液制备:分别精密吸取对照品储备液各5 mL置20 mL棕色量瓶中,加50%甲醇稀释至刻度,摇匀,即得。
2.2.2 供试品溶液 取本品内容物,混匀,研细,取约0.4 g,精密称定,置具塞锥形瓶中,精密加入50%甲醇25 mL,称定质量,超声处理30 min(功率300 W,频率40 kHz ),放冷,再称定质量,用50%甲醇补足减失的质量,摇匀,用微孔滤膜(孔径0.45 μm)滤过,取续滤液,即得。
2.2.3 阴性对照溶液 按广西平乐县中医医院提供的处方比例及制备工艺要求配制分别不含叶下珠、三叶香茶菜药材的阴性对照样品,照“2.2.2”项供试品溶液的制备方法制成阴性对照溶液。
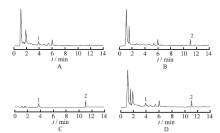
在上述色谱条件下,取混合对照品溶液、供试品溶液、阴性对照溶液,分别进样,色谱图见图1。结果阴性供试品的色谱图分别在没食子酸、齐墩果酸保留时间的相应位置上无干扰峰出现,此方法专属性强,阴性对照无干扰,分离度均>1.5。
精密吸取“2.2.1”项对照品储备溶液1,3,5,7,9 mL,分别置10 mL棕色量瓶中,加50%甲醇至刻度,摇匀,制成不同浓度的混合对照品溶液。取上述不同浓度对照品溶液分别进样,测定峰面积,以浓度( C,μg·mL-1)对峰面积( A)进行线性回归,没食子酸、齐墩果酸的回归方程分别为: A=137.52 C+76.35( r=0.999 6, n = 5), A=154.71 C+18.73( r=0.999 8, n = 5),结果表明,没食子酸、齐墩果酸溶液分别在0.022 06~0.198 54 mg·mL-1,0.031 04~0.279 36 mg·mL-1内与峰面积呈良好的线性关系。
取同一供试品溶液按上述色谱条件连续进样6次,测定峰面积,没食子酸、齐墩果酸的RSD分别为0.56%,0.74%。表明仪器精密度良好。
取同一批号复方黄根颗粒(批号:20130311),按“2.2.2”项方法制备供试品溶液6份,分别测定,计算没食子酸、齐墩果酸各组分含量。结果含量分别为3.71,5.29 mg·g-1,RSD分别为0.56%,0.70%( n=6),表明重复性良好。
取新制备的供试品溶液(批号:20130311 ),分别在0,2,4,6,8,10,12,24 h 进样测定,记录峰面积,没食子酸峰、齐墩果酸峰面积的RSD分别为0.52%,0.71%,表明供试品溶液在24 h内稳定。
精密称取已测定同一批样品(批号:20130311,没食子酸、齐墩果酸的含量分别为3.71,5.29 mg·g-1)0.4 g,置50 mL量瓶中,分别各精密加入没食子酸、齐墩果酸对照品储备溶液5,7,8 mL,按“2.2.2”项供试品溶液的制备方法制备所需要溶液,取供试品溶液和对照品混合溶液各2 μL,分别注入液相色谱仪,计算其加样回收率。没食子酸、齐墩果酸加样平均回收率分别为100.20%和99.96%;RSD分别为0.45%和0.64%。结果见表1。
| 表1 没食子酸和齐墩果酸加样回收率实验结果 Tab.1 Results of recovery tests of gallic acid and oleandic acid |
取复方黄根颗粒的不同批号样品,按“2.2.2”项下的方法制备供试品溶液。精密吸取对照品溶液和供试品溶液各2 μL,注入液相色谱仪,测定,按外标法以峰面积计算样品中没食子酸、齐墩果酸的含量,结果见表2。
| 表2 复方黄根颗粒含量测定结果 Tab.2 Content determination of compound huanggen granule mg·g-1, n=3 |
在实验中,将没食子酸、齐墩果酸对照品混合溶液,在DAD进行全波长紫外扫描,结果没食子酸、齐墩果酸分别在270和215 nm处吸收值最大,并在此波长无干扰,故选择双波长切换。
实验中考察不同比例的甲醇-醋酸水溶液、甲醇-磷酸水溶液、乙腈-磷酸水溶液、乙腈-醋酸水溶液的流动相对该制剂中的没食子酸、齐墩果酸与其他成分的分离效果,最后选定为:以甲醇为流动相A,以0.1%磷酸溶液为流动相B,按本实验设计的梯度洗脱,出峰时间约为3.8和11.2 min,基线稳定,对照品与样品中其他组分达到基线分离,且出峰时间适宜,阴性对照色谱中无干扰峰出现,专属性强,故选择该流动相,结果令人满意。
在提取溶剂考察时分别用不同浓度的甲醇、乙醇为提取溶剂。结果表明,50%甲醇对没食子酸和齐墩果酸提取效率高,故以50%甲醇作为提取溶剂。对提取方法冷浸法、热回流提取法、超声处理法的考察结果表明,超声处理法效果较理想。
实验结果表明,采用UPLC法同时测定复方黄根颗粒中齐墩果酸和没食子酸的含量,具有良好的准确性和重复性,可用于该制剂的质量控制。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|