作者简介: 杨晨(1983-),男,四川绵阳人,助理研究员,硕士,从事药物质量研究工作。电话:028-84216044,E-mail:yangchen@cdu.edu.cn。
通信作者: 任凤英(1975-),女,甘肃静宁人,副研究员,硕士,从事药物质量研究工作。电话:028-84216044,E-mail:renfengying@cdu.edu.cn。
目的 建立顶空气相色谱法同时测定盐酸头孢替安酯原料药中丙酮、乙酸乙酯、异丙醇、二氯甲烷、乙腈5种残留溶剂。方法 采用Agilent DB-624(6%氰丙基苯基-94%二甲基聚硅氧烷固定相)石英毛细管柱(30 m×0.53 mm,3.0 μm),火焰离子化检测仪(FID)检测器, N, N-二甲基甲酰胺(DMF)为溶剂。结果 5种残留溶剂在各自的浓度范围内呈现良好的线性关系( r=0.999 6~0.999 9, n=5),最低检出限范围为0.071~0.847 μg;5种残留溶剂检测的稳定性RSD为 0.40%~2.12%( n=3),平均加样回收率为99.03%~104.79%,RSD为0.54%~3.41%( n=3)。结论 该方法简单、灵敏、可靠,适用于盐酸头孢替安酯原料药中残留溶剂的分析检测。
Objective To establish a method of gas chromatography with head-space sampling for determination of five residual solvents (acetone,ethyl acetate,isopropanol,dichloromethane,acetonitrile) in raw material drug of cefotiam hexetil hydrochloride.Methods Agilent DB-624 capillary column(30 m×0.53 mm,3.0 μm)was used,with FID served as detector and DMF as the solvent.Results Linear relationships were obtained for the 5 residual solvents in their respective concentration ranges ( r=0.999 6-0.999 9, n=5),and the detection range was from 0.071 to 0.847 μg.The stabilities measured as relative standard deviations (RSD) for the 5 residual solvents were from 0.40% to 2.12% ( n=3).The average recovery rates were 99.03% to 104.79%,and RSD were 0.54% to 3.41% ( n=3).Conclusion The method is simple,sensitive and accurate for the residual solvent analysis in raw material drug of cefotiam hexetil hydrochloride.
盐酸头孢替安酯(cefotiam hexetil hydrochloride)为新一代头孢类广谱抗菌药物,对革兰阴性菌和阳性菌都有广泛的抗菌作用。适用对本品敏感的葡萄球菌、链球菌、肺炎球菌、淋球菌、肠道菌属等所致的感染,如扁桃体炎、肺炎、淋巴结炎、乳腺炎、中耳炎等[1,2,3,4]。由于该原料药在制备过程中使用有机溶剂丙酮、乙酸乙酯、异丙醇、二氯甲烷、乙腈,而根据《中华人民共和国药典》2010年版二部附录ⅧP残留溶剂测定法的指导原则和人用药品注册技术规范国际协调会提出的残留溶剂指导原则,这些溶剂均被列为药品必须限制的第二、三类有机溶剂,因此为保证药品质量和用药安全,对该原料药进行有机残留量检测十分重要。由于现有药物合成过程中不能完全去除多余有机溶剂,这些有机溶剂就成为药物中的残留溶剂。利用顶空气相色谱法检测药物中残留溶剂,国内外专家在这个领域中已经取得一定成绩[5,6,7,8,9,10,11,12,13]。笔者在本实验中采用气相色谱顶空进样系统对盐酸头孢替安酯残留溶剂进行研究和测定,报道如下。
Agilent 7890A气相色谱仪(含Agilent G1888顶空进样器,美国安捷伦公司);火焰离子化检测仪(flame ionization detector,FID),KQ-100B超声波清洗仪(工作频率40 kHz,昆山市超声仪器有限公司);Sartorius BP211D分析天平(德国赛多利斯,感量:0.01 mg)。
盐酸头孢替安酯(由成都学院四川抗菌素工业研究所化学部合成,纯度≥97.5%,小试批号:10101901,中试批号:11031101,11031102,11031103);丙酮、乙酸乙酯、异丙醇和二氯甲烷为分析纯(成都市科龙化工试剂厂),乙腈为色谱纯(美国迪马科技公司)。
色谱柱:Agilent DB-624毛细管柱色谱柱(30 m×0.53 mm,3.0 μm);氢火焰离子化检测器:温度为250 ℃;程序升温:40 ℃保持6 min,然后以10 ℃·min-1的速率升温至180 ℃;分流进样,分流比为10:1,进样口温度为200 ℃;载气为氮气,流速为3.0 mL·min-1;顶空进样,顶空平衡温度为80 ℃,顶空平衡时间为30 min,定量环温度为90 ℃,转移管温度为100 ℃;进样体积为1.0 mL。
2.2.1 对照溶液的配制 分别取丙酮、乙酸乙酯、异丙醇、二氯甲烷和乙腈适量,精密称定,加 N, N-二甲基甲酰胺(dimethylformamide,DMF)配制成贮备液;分别取各贮备液适当体积混合后,用DMF稀释成每毫升含丙酮0.25 mg、乙酸乙酯0.25 mg、异丙醇0.25 mg、二氯甲烷0.030 mg、乙腈0.0205 mg的溶液,即为对照品溶液;精密量取对照品溶液2 mL,置于10 mL顶空瓶中,密封,即得。
2.2.2 供试品溶液的配制 分别取3批样品约0.1 g,精密称定,置10 mL顶空瓶中,精密加入DMF 2.0 mL使之溶解,密封,即得。
实验考察3种极性不同的毛细管色谱柱(Agilent DB-624,Hp-5,PEG-20M)对5种残留溶剂的分离效果。结果发现对照品和盐酸头孢替安酯原料药中各残留溶剂采用Agilent DB-624毛细管色谱柱后分离效果较好,并采用程序升温方法,能使对照品与样品中5种残留溶剂达到基线分离。因此,最终选用Agilent DB-624色谱柱作为本实验的分离柱。结果见图1。
本实验固定顶空平衡时间为30 min,对各溶剂在平衡温度为60,70,80,90,100,110 ℃下的色谱响应值(面积)进行实验,结果见图2。可以看出随着平衡温度升高,色谱响应值增大,但平衡温度>80 ℃时,色谱响应值增大趋于平缓。考虑顶空瓶的耐压和气密性等问题会影响测定结果,故本实验选择80 ℃作为平衡温度。
本实验平衡温度为80 ℃,对各溶剂在平衡时间分别为5,10,20,30,40,60 min时的色谱响应值(面积)进行实验,结果见图3。可以看出:平衡时间在30 min后其响应值基本不再增加,说明在30 min时各组分已在气液两相间达到平衡,故本实验选择30 min作为顶空平衡时间。
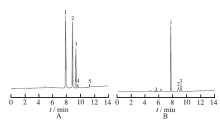 | 图1 标准溶液(A)与样品(B)的色谱图1.丙酮;2.乙酸乙酯;3.异丙醇;4.二氯甲烷;5.乙腈Fig.1 Chromatograms of mixed standard solutions (A) and sample (B)1.acetone;2.ethyl acetate;3.isopropanol;4.dichloromethane;5.acetonitrile |
 | 图2 5种溶剂在不同平衡温度的响应值Fig.2 Response value of five kinds of solvent at different equilibrium temperature |
分别取丙酮、乙酸乙酯、异丙醇、二氯甲烷和乙腈各适量,精密称定,加DMF配制成贮备液;分别取各贮备液适当体积混合后,用DMF稀释成每毫升中含丙酮、乙酸乙酯、异丙醇各1.25 mg、二氯甲烷0.150 mg和乙腈0.102 mg的溶液,即为标准溶液Ⅰ;精密量取标准溶液Ⅰ,用DMF依次稀释5,25,125和625倍,得标准溶液Ⅱ、Ⅲ、Ⅳ和Ⅴ。精密量取标准溶液Ⅰ、Ⅱ、Ⅲ、Ⅳ和Ⅴ各2 mL,分别置于10 mL顶空瓶中,密封,在以上色谱条件下测定,记录各溶剂的保留时间和峰面积。以对应溶剂的检出量和峰面积计算线性关系。将对照溶液(标准溶液Ⅱ)多次稀释,并在以上色谱条件下进行测定,以信噪比为3时,计算最低检出限,以信噪比为10时,计算定量限,结果见表1。
| 表1 5种溶剂的线性关系、检出限和定量限 Tab.1 Linear regression, the limit of detection and quantification for five kinds of solvent |
精密量取标准溶液Ⅱ2 mL,置于10 mL顶空瓶中,密封,按上述条件顶空进样6次,结果测得丙酮RSD为1.34%,乙酸乙酯RSD为1.38%,异丙醇RSD为2.00%,二氯甲烷RSD为1.43%,乙腈RSD为2.18%。结果表明,该色谱条件下仪器精密度良好。
将标准溶液Ⅱ分别于1 h,2 h,4 h,8 h,1 d,2 d后分别进样分析,以各溶剂测得的峰面积的RSD衡量日间测定的重复性,结果测得丙酮RSD为1.26%,乙酸乙酯RSD为0.84%,异丙醇RSD为0.40%,二氯甲烷RSD为1.96%,乙腈RSD为2.12%。结果表明,该色谱条件下溶液稳定性良好。
称取小试批号10101901样品0.1 g,精密称定,置于10 mL顶空瓶中,分别精密加入对照品溶液1.6,2.02.4 mL,密封,超声10 min使溶解,即得。按照“2.6”项方法进样分析,结果见表2。
| 表2 5种溶剂回收率实验结果 Tab.2 Results of recovery test on five kinds of solvent |
精密称取4批样品(小试批号10101901,中试批号:11031101,11031102,11031103)0.1 g置10 mL顶空瓶中,精密加入DMF 2.0 mL,混匀,密封,按上述条件顶空进样,记录色谱图和峰面积,以外标法计算3批样品中的残留溶剂含量均在限度以下,结果见表3。
| 表3 盐酸头孢替安酯原料药残留溶剂的分析结果 Tab.3 Analytical results of residual solvent in bulk drug of cefotiam hexetil hydrochloride % |
研究结果表明,本实验所建立的残留溶剂检测方法简单,快速,准确,有效,符合药品中残留溶剂的测定,适合不同生产企业及有关检测机构对盐酸头孢替安酯原料药进行质量控制,同时也可为从事多组分残留溶剂检测的分析工作者提供参考。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|



