作者简介: 肖敏(1988-),女,湖南娄底人,医师,硕士,主要从事肾脏疾病的基础研究电话:0755-29589545,E-mail:25790749@qq.com。
通信作者: 尹友生(1957-),女,湖南邵阳人,主任医师,教授,硕士生导师,主要从事肾脏疾病的基础及临床研究。电话:0773-2810226,E-mail:yinyousheng@163.com。
目的 观察雷洛昔芬对氯化镉染毒肾小管上皮细胞中雌激素受体α(ERα)、ERβ和金属硫蛋白-1a(MT-1a)基因表达的影响,并探讨其机制。方法 选取新生Sprague Dawley(SD)大鼠的肾脏组织进行细胞培养,采用Percoll法分离纯化肾小管后原代培养。选取第2代细胞进行实验。实验分为空白对照组、氯化镉组、雷洛昔芬组。4 h后采用噻唑蓝(MTT)法检测细胞活力,24 h后应用反转录聚合酶链反应(RT-PCR)及免疫组化检测ERα、ERβ及MT-1a mRNA及蛋白水平。结果 与空白对照组比较,氯化镉组大量细胞的形态发生改变,细胞大量死亡,存活率为55.3%,同时ERβ,MT-1a mRNA及蛋白表达水平升高( P<0.05);与氯化镉组比较,雷洛昔芬组仅少量细胞形态发生改变,存活率88.6%,ERβ,MT-1a mRNA及蛋白表达水平下降( P<0.05)。 而ERα表达在3组间变化不明显,差异无统计学意义( P>0.05)。结论 雷洛昔芬可竞争性与ERβ结合,下调MT-1a的表达,减少Cd-MT复合物的形成,而降低镉对肾小管上皮细胞的损伤。
Objective To investigate the effect of raloxifene on ERα,ERβ and MT-1a expression in renal tubular epithelial cells contaminated with cadmium chloride,for exploring action mechanism.Methods Renal tubule cells were isolated from kidneys of new born SD rats and purified by Percoll.The cells of the second generation were selected for experiment.The cells were divided into 3 groups:blank control group,cadmium chloride group and raloxifene group.After 4 h,cell viability was detected by MTT,and after 24 h,mRNA and protein expression levels of ERα,ERβ and MT-1a in renal tissues were determined by RT-PCR and immunohistochemistry technology,respectively.Results Compared with the blank control group,morphology of plenty cells were changed in cadmium chloride group,a number of cells were dead,and the survival rate was only 55.3%;at the same time,mRNA and protein expression levels of ERβ and MT-1a significantly increased ( P<0.05).Compared with cadmium chloride group,only a small part of cells underwent morphological changes,and the survival rate was 88.6% in raloxifene group,and the mRNA and protein expression levels of ER β and MT-1a were significantly decreased ( P<0.05).The expression of ERα showed no significant difference among the three groups ( P>0.05).Conclusion Raloxifene can bond with ERβ competively,down-regulate MT-1a and decrease Cd-MT synthesis,so as to reduce cadmium-induced injury of renal tubular epithelial cells.
镉(cadmium,Cd)对哺乳动物具有多重毒性作用,其损伤呈多系统、多器官性[1]。肾脏是镉毒性的主要靶器官之一。然而,镉所致肾毒性的分子机制尚不明确。国内外研究者对镉肾毒性的研究多以动物实验和细胞系研究为主,原代培养研究较少。而原代细胞培养更接近和反映体内生长特性,更适合进行毒理学研究[2]。研究发现,镉具有类雌激素作用,能模拟雌激素与雌激素受体(estrogen receptor,ER)结合从而发挥毒性作用[3]。雷洛昔芬(raloxifene)作为选择性雌激素受体调节剂,可选择性与雌激素受体结合从而发挥类雌激素或抗雌激素作用。本课题的前期实验,通过雷洛昔芬治疗镉染毒去卵巢大鼠发现,雷洛昔芬可明显降低镉对肾脏的损害,但其作用机制尚不明确。因此,笔者通过本实验在建立大鼠肾小管上皮细胞原代培养的基础上,研究镉对肾小管上皮细胞损伤的机制及雷洛昔芬的保护机制。
新生3 d内的Sprague Dawley(SD)乳鼠,清洁级,雌雄兼用,由桂林医学院实验动物中心提供,动物生产许可证号:SCXK(桂)2012-0001,实验动物使用合格证号:SYXK(桂)2012-0001。室温(20±2) ℃,相对湿度55%~65%。
低糖无酚红DMEM培养液(批号:SH30021.01B)、胰酶(批号:SH40003-12)、胎牛血清(批号:SV30087.02),均购自Hychone公司;氯化镉(成都市科龙化工试剂厂,批号:GB/T1285-94);雷洛昔芬(大连美仑生物公司,批号:20120301);反转录聚合酶链反应(RT-PCR,TaKaRaExTap公司,批号:DRR047A);上下游引物(上海生工公司合成,批号:HG1212240013);ERα,ERβ小鼠抗大鼠单克隆抗体(ABZOOM公司,批号:AB-0174R);金属硫蛋白-1a(MT-1a)鼠抗人金属硫蛋白单克隆抗体(北京中杉金桥生物技术有限公司,批号:ZS-2044)。
基因扩增仪(英国Techne公司,批号:TC-512);凝胶分析系统(南宁精密仪器仪表有限公司,型号:JS-380);光学显微镜(日本奥林巴斯公司);Image Pro Plus 6.0图像分析系统(美国Media Cybernetics公司);酶标仪(美国伯乐公司,MLDEL680)。
新生3 d内SD乳鼠10只,置入75 %乙醇中浸泡5 min。无菌取双肾,去除肾蒂及包膜,将肾皮质剪碎至1 mm3大小,用0.25%胰蛋白酶和1 g·L-1Ⅰ型胶原酶震荡消化6 min,未消化的肾皮质再次进行消化,反复操作5或6次后至无组织残留。将消化后的细胞悬液分别移至孔径0.150 mm(100目)、0.075 0 mm(200目)筛网滤过后,900 r·min-1离心6 min( r=13.5 cm)。离心后弃上清液,将细胞沉淀用达尔伯克改良伊格尔培养液(DMEM)制成细胞悬液4 mL。取预先配好45% Percoll分离液,将细胞悬液轻轻铺于其上,13 000 r·min-1( r=13.5 cm),4 ℃条件下离心30 min。吸取近管底第2层细胞悬液,即为近端肾小管节段及其游离的上皮细胞。将分离纯化的肾小管上皮细胞阶段用DMEM离心洗涤,1 000 r·min-1离心10 min,共2次。将分离的近端肾小管上皮细胞用含10%胎牛血清的DMEM培养液重悬后接种于培养皿中,于37 ℃,5% 二氧化碳(CO2)孵箱中静置培养,隔天换液。原代培养4~5 d后细胞长满,传代,继续培养。
将第2代的细胞分为3组:空白对照组,氯化镉组,雷洛昔芬组。空白对照组:培养液中加入等体积磷酸盐缓冲液(PBS)。氯化镉组:培养液中加入50 μmol·L-1氯化镉(研究发现镉的毒性效应呈剂量依赖性,50 μmol·L-1氯化镉的毒性大于20,30及40 μmol·L-1氯化镉的毒性[6],故本实验选择50 μmol·L-1氯化镉)。雷洛昔芬组:培养液中加入50 μmol·L-1氯化镉和5 μmol·L-1雷洛昔芬溶液[本实验的前期研究通过予不同浓度的雷洛昔芬(3,4,5,6 μmol·L-1)干预镉染毒后的肾小管上皮细胞,细胞的存活率依次为70.3%,78.5%,84.9%,80.6%,说明5 μmol·L-1雷洛昔芬存活率最高,故本实验采用5 μmol·L-1雷洛昔芬干预。
培养的第2代肾小管上皮细胞以1×105个·mL-1接种于96孔板,24 h后在培养液中加入上述DMEM 稀释的雷洛昔芬及氯化镉溶液,每组做4个复孔。 染毒结束前4 h,每孔加入5 g·L-1MTT 20 μL,继续培养。染毒结束后吸弃孔内培养液,加入二甲亚砜(DMSO)150 μL,振荡10 min,待充分溶解结晶后,在酶标仪上以波长490 nm测吸光度( A值),并计算细胞相对存活率。细胞相对存活率(%)=(实验组 A值/空白对照组 A值)×100%。
培养第2代肾小管上皮细胞分为3组,以1×105个·mL-1接种于培养皿中,待细胞培养至70%~80%后,用PBS清洗,换用含有胎牛血清的DMEM培养液,并按“1.5”项分组分别加入相应浓度的氯化镉及雷洛昔芬,继续培养24 h后,用基因扩增仪进行PCR扩增。扩增引物:ERα引物序列:上游5'-GACATGTTGCTGGCTACGTC-3',下游5'-GGCCATCAAGTGGATCAAAG-3',扩增片段大小为198 bp;ERβ引物序列:上游5'-AAAGTAGCC-GGAAGCTGACAC-3',下游5'-TACACCGGGACCACA-TTTTTG-3',扩增片段大小为202 bp;MT-1a引物序列:上游5'-ACCGTTGCTCCAGATTCACC-3',下游5'-CACTTGTCCGAGGCACCTT-3',扩增片段大小为200 bp;GAPDH引物序列:上游5'-CCAGAACATCATCC-CTGCCTC-3',下游5'-TAGCCAAATTCGTTGTCATACCA -3',扩增片段大小为351 bp。ERα,ERβ反应条件为预变性94 ℃,2 min→变性94 ℃,30 s →退火58 ℃,30 s→延伸72 ℃,90 s,38个循环后于72 ℃延伸10 min,最后4 ℃保存。MT-1a及甘油醛-3-磷酸脱氢酶(GAPDH)反应条件为预变性 94 ℃,2 min→变性 94 ℃,30 s →退火 55 ℃,30 s→延伸72 ℃,90 s,30个循环后于72 ℃延伸10 min,最后4 ℃保存。 ERα,ERβ及MT-1a表达量分别以目标条带 A 值/GAPDH A值表示并记录。
取对数生长期的细胞悬液滴加在多聚赖氨酸处理的无菌载玻片上,待细胞爬满载玻片后,用多聚甲醛固定细胞爬片15 min,PBS冲洗3 min,3次,3%过氧化氢(H2O2)室温孵育10 min,PBS冲洗3 min,3次,滴加一抗封闭细胞爬片,37 ℃,60 min,PBS冲洗3 min,3次,滴加二抗,室温孵育15 min,PBS冲洗3 min,3次,二氨基联苯胺(DAB)显色3~10 min,立即用自来水冲洗,中止显色,苏木精复染,分化,返蓝,脱水,干燥,封片。使用医学图像分析系统采集分析图像数据。每张细胞爬片随即选取视野3个,计算累积分吸光度值( IA)。
采用SPSS 17.0版统计软件进行分析,计量数据以均数±标准差(
空白对照组肾小管上皮细胞呈梭型紧贴瓶底,氯化镉组细胞大量死亡,大部分细胞失去正常的细胞形态,呈圆形,且漂浮于瓶底。雷洛昔芬组的细胞死亡减少,仅少部分细胞的形态异常。
与空白对照组 A值(0.132±0.013)比较,氯化镉组 A值(0.073±0.014)明显下降,差异有统计学意义( t=12.122, P<0.05),细胞存活率为55.3%。与氯化镉组比较,雷洛昔芬组 A值(0.117±0.027)明显上升,差异有统计学意义( t=12.122, P<0.05),细胞存活率为88.6%。
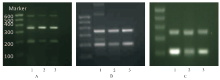
2.3 3组细胞ERα、ERβ、MT-1a mRNA的相对表达强度
3组细胞ERα、ERβ、MT-1a的mRNA表达强度的测定结果见图1和表1。与空白对照组比较,氯化镉组ERβ、MT-1a的mRNA表达量明显上升( P<0.05)。与氯化镉组比较,雷洛昔芬组ERβ,MT-1a mRNA表达量有所下降( P<0.05)。而ERα的表达量变化不明显,组间比较差异无统计学意义( P>0.05)。
| 表1 3组肾小管上皮细胞ERα、ERβ、MT-1a的 A值变化 Tab.1 Variation of A value of ERα, ERβ and MT-1a in three groups of renal tubular epithelial cells |
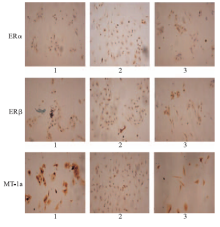
2.4 3组细胞ERα、ERβ、MT-1a免疫组化的相对表达强度
经免疫组化测定,ERα与ERβ阳性表达主要位于细胞胞核内,少量位于细胞质内呈棕黄色。MT-1a阳性表达位于细胞质内呈棕黄色(图2)。经吸光度测定,3组ERα、ERβ、MT-1a蛋白的表达量与mRNA表达相似。经氯化镉染毒的细胞,其ERβ、MT-1a的mRNA表达量明显上升( P<0.05)。给予雷洛昔芬后,ERβ,MT-1a mRNA表达量有所下降( P<0.05)。而ERα的表达量未见明显改变,组间比较差异无统计学意义( P>0.05)(表2)。
| 表2 3组肾小管上皮细胞ERα、ERβ、MT-1a表达变化 Tab.2 Variation of the expression of ERα, ERβ and MT-1a in three groups of renal tubular epithelial cells |
镉作为主要的工业和环境污染物之一,可通过呼吸道和消化道进入体内。而肾脏可吸收进入体内近1/3的镉,是镉聚集最重要的靶器官之一[4]。研究发现,低剂量接触镉主要引起以近曲小管损害为主要特征的肾损害[5]。国内外大量研究表明,镉对体外培养的肾小管上皮细胞有直接毒性损伤,且毒性效应呈剂量和时间依耐性[6,7]。本实验通过使用50 μmol·L-1氯化镉染毒肾小管上皮细胞后细胞大量死亡,大部分细胞失去正常的细胞形态,MTT法测定细胞毒性作用的实验中显示细胞的生长明显受到抑制。说明小剂量氯化镉就可引起细胞的广泛死亡,肾小管上皮细胞对镉的损害很敏感。
目前国内外对镉致肾损伤机制还未明确。MT-1a是体内分布最广泛的金属硫蛋白功能亚型,主要表达于细胞质内。其对重金属离子具有较高的亲和力,其表达量的高低可反应肾功能的损害程度[8]。近期有研究发现,MT-1a可与镉结合,形成Cd-MT形式,是镉产生毒性作用的主要存在形式。逢兵等[9]证实,肾皮质中MT1及MT2基因表达水平分别与肾皮质中镉的含量呈正相关,且MT1及MT2基因表达与Cd-MT呈剂量-效应关系。由此表明,MT-1a在镉的肾毒性中产生关键性作用。笔者在本实验观察到,给予氯化镉染毒细胞后,MT-1a mRNA及蛋白的表达量均明显升高,表明镉可能刺激肾小管上皮细胞中的MT-1a表达后与其结合形成Cd-MT化合物,从而介导细胞死亡。而有研究发现,MT 是一种雌激素应答基因,其表达可以由ER的表达介导。HOFER等[10]分别给大鼠注射氯化镉和雌二醇发现,氯化镉和雌二醇都能使肾脏组织MT-1a的表达量增加。表明ER是MT-1a的上游因子,可调节MT-1a表达。
ER在生物体内主要有ERα和ERβ两种亚型,广泛分布在全身各组织中,那么MT-1a在肾小管上皮细胞中是有哪种ER受体介导,镉作为一种类雌激素,可与哪种ER受体结合,目前国内外研究较少。近年来有研究发现,镉具有类雌激素作用,能模拟雌激素与ER结合,可改变ER水平[2]。ISHITOBI等[11]将围生期孕鼠给予含量为10 ppm的镉污染的饮水喂养,即可检测到其子代脑部ERα mRNA、ERβ mRNA表达下调。本课题的前期研究发现,通过氯化镉染毒去卵巢大鼠后,其肾脏组织中的ERβ表达量明显比空白对照组升高。表明镉在肾脏组织中可结合ERβ。本实验也证实此点,给予氯化镉后MT-1a及ERβ mRNA及蛋白的表达量明显增高( P<0.01),ERα表达量增加不明显( P>0.05)。说明镉通过结合ERβ,刺激其下游因子MT-1a的表达,从而介导肾小管上皮细胞的损伤。
雷洛昔芬作为第二选择性雌激素受体调节药,可选择作用于不同组织的不同雌激素受体而发挥类雌激素或抗雌激素作用。刘立朝等[12]发现,雷洛昔芬可上调ERαmRNA基因表达抑制破骨细胞骨吸收,发挥类雌激素作用从而治疗骨质疏松。本研究结果显示,给予雷洛昔芬后细胞死亡减少,仅少部分细胞的形态异常,MTT测定结果显示细胞存活率明显提高。说明雷洛昔芬对于镉染毒肾小管上皮细胞存活率的下降有一定的保护效应。这可能与雷洛昔芬调节ER有关。本研究还发现,雷洛昔芬组的ERβ、MT-1a的mRNA及蛋白的表达量比氯化镉组明显下降( P<0.01),ERα表达量未见明显变化( P>0.05)。说明雷洛昔芬在肾小管上皮细胞中主要是与镉竞争性结合ERβ,而非ERα。
综上所述,笔者初步推测,镉对肾小管上皮细胞的损伤机制可能是其与细胞中ERβ结合后,上调MT-1a表达,与镉结合形成Cd-MT化合物,从而介导细胞损伤。而雷洛昔芬作为选择性雌激素调节药,可与镉竞争性结合ERβ受体,减少细胞对MT-1a的表达而降低镉对肾小管上皮细胞的损伤作用。由于本实验采用的是半定量测定的方式,且缺乏临床实验研究,其机制还有待进一步探讨。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|