作者简介: 周保柱(1990-),男,安徽舒城人,在读硕士,研究方向:高原特殊环境损伤与防治。电话:0931-8994676,E-mail:zhoubz2014@sina.com。
通信作者: 贾正平(1957-),男,山西忻州人,主任药师,教授,博士,研究方向:高原特殊环境损伤与防治。电话:0931-8994676,E-mail:limaox2005@aliyun.com。
目的 探讨 L-亮氨酸对高原记忆损伤的改善作用及其机制。方法 通过八臂迷宫筛选雄性昆明种小鼠50只,随机分为常氧对照组(NC组),模型对照组(Model组), L-亮氨酸小、中、大剂量组。 L-亮氨酸小、中、大剂量组分别按0.473, 0.945,1.89 g·kg-1剂量灌胃给予 L-亮氨酸,NC组和Model组给予等体积纯化水。均给药1周。给药第4天,将Model组和 L-亮氨酸小、中、大剂量组置于大型低压氧舱模拟高原低压低氧环境(海拔7 500 m,3 d)。采用八臂迷宫测试其空间学习记忆能力;干/湿比重法测定各组脑组织含水量变化;苏木精-伊红(HE)染色观察海马CA1区细胞形态变化;SYBR Green 实时定量PCR检测海马组织mTOR、P70S6K和4E-BP1 mRNA表达。结果 与NC组比较,Model组参考记忆错误(RME)、错误总数(TE)及测试时间(TT)均显著增加( P<0.05),脑含水量显著升高( P<0.01),海马CA1区神经元损伤加重,mTOR和P70S6K mRNA表达显著降低( P<0.05)。与Model组比较, L-亮氨酸小、中剂量组工作记忆错误(WME)、RME、TE、TT、脑含水量和4E-BP1 mRNA表达均降低,P70S6K mRNA表达增加; L-亮氨酸大剂量组WME和TE均显著降低( P<0.05),脑含水量显著降低( P<0.01),P70S6K mRNA表达显著增加( P<0.05)。 L-亮氨酸小、中、大剂量组海马CA1区神经元损伤明显减轻。结论 L-亮氨酸对高原记忆损伤有改善作用,其机制可能通过激活mTOR及其下游底物(4E-BP1和P70S6K)发挥作用。
Objective To explore the improving effect of L-leucine on memory impairment in plateau and the mechanism.Methods After successfully trained in the 8-arm radial maze,50 male Kunming mice were selected and randomly divided into normoxic control group (NC group),model group,and L-leucine (low,medium and high dose) groups.Animals in L-leucine groups were intragastrically given 0.473 g·kg-1,0.945 g·kg-1and 1.89 g·kg-1 L-leucine for 7 days and those in NC and model control groups were administered the same volume of purified water for the same period of time.At the 4th day of the treatment,the mice in the model control group and L-leucine groups were placed in a large low-pressure and low-oxygen chamber to simulate low-pressure hypoxic environment of the plateau (7 500 m,3 d).The 8-arm radial maze was used to measure the spatial learning and memory ability of mice and dry-wet method to measure the water content of brain tissue.HE staining was employed to observe the cell morphological changes in CA1 region of the hippocampus.The expression levels of mTOR,P70S6K and 4E-BP1 mRNA in the hippocampus were detected by SYBR Green real-time PCR.Results The reference memory error (RME),total error (TE),testing time (TT),and water content of brain tissue were significantly increased,the neuron injury was exacerbated in CA1 region of the hippocampus,and the expression levels of mTOR and P70S6K mRNA were markedly decreased in model control group when compared with those in NC group ( P<0.05 or P<0.01).These indexes,however,were significantly improved in L-leucine groups,especially in high-dose group.Condusion L-leucine can improve memory impairment in plateau,and the mechanism may involve the activation of mTOR and its downstream substrates (4E-BP1 and P70S6K).
高原环境对认知功能的损伤严重影响高原人群的工作与生活。主要表现在知觉、学习记忆功能、注意力、语言功能、人格以及情绪等方面,并且其作用与海拔高度、进入高原时间和任务复杂程度明显相关[1],但高原缺氧致记忆损伤的神经生理学作用机制尚不清楚。因此,如何有效降低高原低压低氧对记忆的损伤,已成为需特别重视并加以解决的问题。
哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)是存在于细胞质中的一种丝/苏氨酸蛋白激酶,参与蛋白质翻译、细胞凋亡和神经突触可塑性等多种生物学功能。近年来研究发现,mTOR信号通路与学习记忆损害和高原损伤特征相关。EHNINGER等[2]研究发现,增强mTOR-Raptor的功能可提高脑长时记忆功能。笔者在构建高原低压低氧模型基础上,采用mTOR激动药 L-亮氨酸干预,继而从行为学、形态学和分子生物学等方面探讨 L-亮氨酸对高原记忆损伤的改善作用,以期进一步阐明 L-亮氨酸改善高原记忆损伤的作用机制。
RM-200八臂迷宫分析测试系统(成都泰盟科技有限公司);DYC-3070大型低压氧仓(贵州风雷航空军械有限公司);System9700 PCR仪;ABI7300荧光定量PCR仪;生物显微镜及照相系统(Olympus,XI-170); L-亮氨酸购自上海美克林公司(纯度:99%),柱式法Total RNA提取试剂盒(制品名称:TaKaRa MiniBEST Universal RNA Extraction Kit,批号:9767);反转录试剂盒(制品名称:PrimeScriptTMRT Maser Mix, 批号:RR036A);SYBY Green 购自TaKara公司;RT-PCR所用引物均委托TaKara公司合成。
SPF级健康雄性昆明种小鼠75只,体质量20~22 g,购于兰州大学实验动物中心,生产许可证号:SCXY(甘)2013-0002,动物合格证号:NO.62000800000023。饲养室控制室温(22±1)℃,每12 h明暗交替,标准饲料喂养,自由饮水,在进行八臂迷宫实验前限制小鼠饮食,使其体质量维持在自由进食时的80%~85%。
训练前小鼠先在迷宫中适应2 d,每天2次。适应时将3或4只小鼠置于迷宫,自由摄取食物5 min。适应训练后,只在迷宫中4个臂(1,3,4,7臂)放置食物和信号图片,并维持此顺序至实验结束。将小鼠置于迷宫中央区,关闭15 s后将门打开让小鼠自由觅食,直至3 min末或提前完成所有臂的觅食,即结束一次训练。测试指标:①工作记忆错误(working memory errors,WME),即在同一次训练中动物再次进入已经吃过食物的臂;②参考记忆错误 (reference memory errors,RME),即动物进入不曾放过食物的臂;③错误总数(total errors,TE),即在3 min内出现错误的总数;④测试时间(the total reaction times,TT),即动物吃完所有食物所花的时间。连续5次TE≤1,同时WME=0为训练成功(连续训练20 d)。
将八臂迷宫训练成功的昆明种小鼠50只随机分为5组:常氧对照组(NC组)、模型对照组(Model组)、 L-亮氨酸小剂量、 L-亮氨酸中剂量组、 L-亮氨酸大剂量组,每组10只。自分组起,连续灌胃7 d,每天1次,NC组和Model组灌胃纯化水, L-亮氨酸小、中、大剂量组分别按0.473,0.945,1.890 g·kg-1 L-亮氨酸灌胃。剂量参考FUMIAK等[3]实验结果和实验动物剂量换算公式。
给药第4天,除NC组外,其余各组均置于大型低压氧舱中模拟海拔7 500 m高原环境(舱内压强:35.9 kPa,氧分压:8.0 kPa),每天9:00以10 m·s-1速度下降至4 000 m(舱内压强:62.1 kPa,氧分压:13.0 kPa),实验人员进舱,在舱里灌胃给药,换水、食和垫料,连续3 d,每天给药完毕后,将舱内高度以10 m·s-1的速度匀速上升到预定海拨(7 500 m),在此期间动物自由摄食及饮水。NC组小鼠于动物房同时饲养。
造模后,八臂迷宫实验观察小鼠空间记忆能力以判定模型成败。八臂迷宫测试系统纪录分析各组小鼠WME、RME、TE及TT,每只小鼠测试两次,取平均值。
从各组随机抽取小鼠5只,处死,迅速断头取脑,矢状位对称切开全脑,去除小脑和脑干。切取右侧脑组织标本,常规固定、石蜡包埋,4 μm切片,裱于经多聚赖氨酸包埋的清洁载玻片上,常规脱蜡、复水、磷酸盐缓冲液(PBS)洗涤,苏木精-伊红(HE)染色。取剩余左脑组织精确称重,放入恒温烘干箱100 ℃烘烤24 h至恒重,称取干脑质量,按Eilliott公式计算:脑组织含水量(%)=(湿重-干重)/湿重×100%。
处死各组剩余小鼠,剖取海马组织样本,即刻冻存于-80 ℃冰箱。参考柱式法Total RNA提取试剂盒(制品名称:TaKaRa MiniBEST Universal RNA Extraction Kit,批号:9767)说明书提取样本总RNA,采用 A260 nm/ A280 nm分光光度法检测RNA纯度及浓度。逆转录cDNA采用10 μL反应体系,其条件为37 ℃,15 min,85 ℃失活5 s。SYBR Green 实时定量PCR采用10 μL反应体系,条件95 ℃预变性30 s;95 ℃反应5 s,60 ℃退火31 s,重复40个循环,每个样本做3个复孔,以GAPDH为内参基因,计算各组小鼠海马mTOR、P70S6K和4E-BP1的△Ct,目的基因相对表达量采用2-△△Ct进行计算分析。本实验中mTOR、P70S6K、4E-BP1和GAPDH引物序列见表1。
| 表1 P70S6K、mTOR、4E-BP1和GAPDH引物序列 Tab.1 Primer sequence of P70S6K, mTOR, 4E-BP1 and GAPDH |
采用SPSS13.0版统计软件进行统计学处理,结果以均数±标准差(
与NC组比较,Model组RME、TE及TT显著增加( P<0.05),WME亦增加; L-亮氨酸小、中剂量组RME、TE和TT均显著增加( P<0.05); L-亮氨酸大剂量组WME、RWE、TE和TT均有增加趋势。与Model组比较, L-亮氨酸小、中剂量组WME、RWE、TE和TT均有降低趋势,差异无统计学意义; L-亮氨酸大剂量组WME和TE均显著降低( P<0.05),RME和TE有降低趋势,见表2。
| 表2 5组小鼠八臂迷宫实验结果 Tab.2 Results of eight-arm radial maze test in five groups of mice 次, n=10, |
与NC组比较,Model组脑组织含水量显著升高( P<0.01),提示高原低压低氧模型制备成功。与Model组比较, L-亮氨酸各剂量组小鼠脑组织含水量均降低( P<0.05或 P<0.01),其中大剂量组最明显( P<0.01),见表3。
| 表3 5组小鼠脑组织含水量测定结果 Tab.3 Determination results of water content in brain tissue of five groups of mice n=5, |
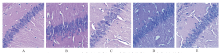
NC组海马CA1区结构清晰,细胞形态正常,布局有序,神经元无损伤丢失,胞体、胞核清晰,核仁清楚。Model组海马CA1细胞层数减少,细胞脱失明显,细胞间隙增大,神经胶质细胞呈网状和条索状增生,神经元排列散乱、稀疏。 L-亮氨酸各剂量组均有少量神经元丢失及胶质增生,但细胞形态较正常,细胞层数无明显减少,见图1。
与NC组比较,Model组mTOR和P70S6K mRNA表达显著降低( P<0.05),4E-BP1 mRNA表达增加; L-亮氨酸小、中、大剂量组mTOR和P70S6K mRNA表达显著降低( P<0.05),4E-BP1 mRNA表达显著性增加( P<0.05)。与Model组比较, L-亮氨酸各剂量组的P70S6K mRNA表达均有增强趋势,其中大剂量作用最明显( P<0.05);4E-BP1 mRNA表达均有降低趋势,见图2。
mTOR是调控蛋白质翻译起始阶段一种蛋白激酶,是多种信号转导的“整合器”,参与基因转录、蛋白质翻译起始、核糖体生物合成、细胞凋亡等多种生物学功能。高原低压低氧能够直接激活DNA损伤反应调节基因1(REDD1),也能通过激活低氧诱导因子(HIF)直接控制REDD1/RTP801的基因表达,提高TSC1/2的活性,进而抑制mTOR激活[4]。低氧能够抑制能量生产,造成能量应激,使AMP升高,激活AMPK/TSC2信号通路,从而抑制mTOR[5]。另外,高原低氧导致的氧化应激因子(reactive oxygen species,ROS)生成增加也能影响mTOR通路[6]。
研究发现,mTOR在神经元突触可塑性和记忆保护中起重要作用[7]。在脑不同区域,如海马CA1区、齿状区、纹状体等脑区的研究均表明mTOR参与了长时程增加效应(long-term potentiation,LTP)维持阶段,对晚时相LTP必不可少[8]。活化mTOR能够激活下游底物4E-BP1 和S6K1,增加AMPA受体在膜表面表达,促进谷氨酸转运体3(excitatory amino-acid transporter 3,EAAT3))对谷氨酸的摄取,从而减少神经兴奋性毒性[9]。mTOR-Raptor激活一系列在突触可塑性中起到重要作用的蛋白质[1],如突触素(synaptophysin,SYP)、突触后致密物(postsynaptic density protein 95,PSD-95)。因此,激活mTOR及其底物在减少神经元和记忆损伤上起非常重要的作用。
本实验采用 L-亮氨酸干预高原低压低氧模型,该模型能够模拟高原记忆损伤。造模后,Model组空间学习和记忆能力明显降低,脑含水量明显升高,海马CA1神经元严重损伤,mTOR和P70S6K mRNA明显降低,4E-BP1 mRNA表达增加,说明高原低压低氧模型造模成功,这与文献[4,6]报道相符。
本实验研究结果显示, L-亮氨酸对高原记忆损伤具有一定的改善作用,主要表现:① 改善Model组学习记忆能力,②减少脑含水量,③减轻海马CA1神经元损伤,④激活mTOR下游底物4E-BP1和P70S6K的磷酸化。DANIELE等[10]研究发现海马组织mTOR下游底物P70S6K磷酸化,能够调节蛋白质翻译,参与长时记忆的形成。mTOR下游底物另一主要成分4E-BP1磷酸化与海马神经元的多种神经元活动有关,包括脑源性神经营养因子诱发的突触电位增强[11]。共同作用于学习和记忆神经生物学过程,发挥保护神经元和促进小鼠学习记忆恢复的作用,同时也进一步表明以激活mTOR及其底物为切入点来改善高原记忆损伤具有一定的可行性。
综上所述, L-亮氨酸对高原记忆损伤有改善作用,可降低脑含水量,减轻海马组织CA1神经元损伤并提高空间学习记忆能力,其机制可能通过激活mTOR及其下游底物发挥作用。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|